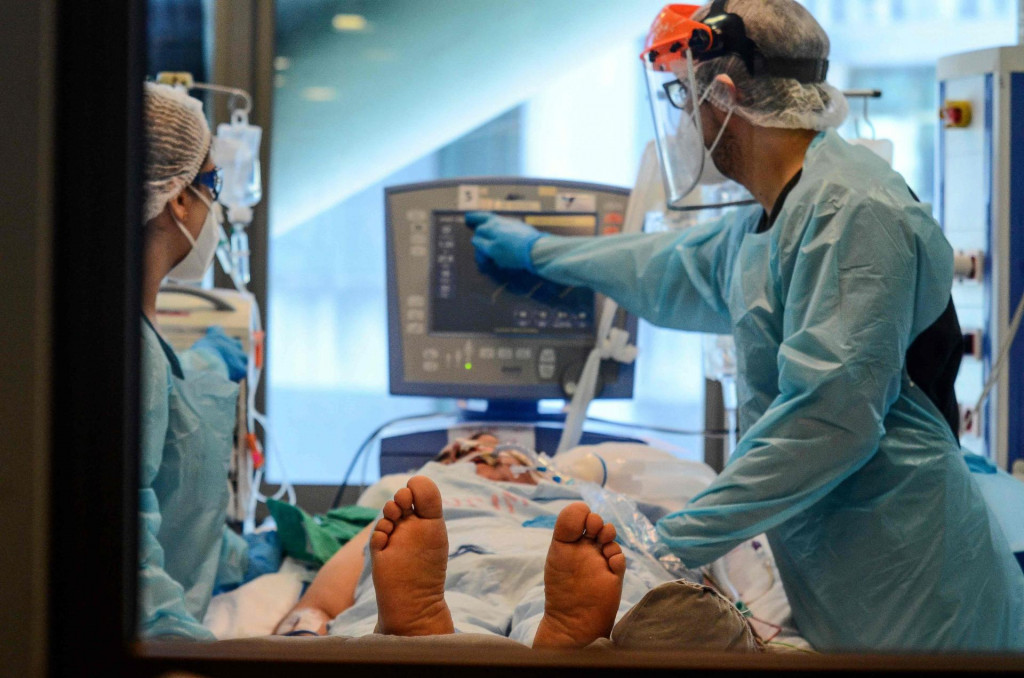
Utrka svjetskih proizvođača cjepiva protiv koronavirusa ulazi u samu završnicu: zalog nije samo znanstvena slava i zaustavljanje opake globalne pandemije, nego – povrh svega - i nezamislivo vrtoglava zarada.
Britanska vlada već je odobrila upotrebu cjepiva tvrtki Pfizer/BioNTech protiv koronavirusa i s cijepljenjem počinje uskoro, objavio je BBC. Cjepivo kojemu je navodno utvrđena 95-postotna učinkovitost Britancima će možda biti dostupno već od sljedećeg tjedna, a prva narudžba iznosi 800.000 doza.
Već i laicima je pomalo čudno što je američki farmaceutski div Pfizer odobrenje za upotrebu svoga cjepiva prije dobio u Velikoj Britaniji nego u svojoj matičnoj zemlji, no tajna primarno leži u propisanoj proceduri: velik broj europskih agencija za lijekove oslanja se na analizu...